宿主細胞DNA(Host Cell DNA)是指用于生產(chǎn)生物制品(如重組蛋白�、疫苗、生物藥物等)細胞中的遺傳物質(zhì)��。在生物技術(shù)和生物制藥行業(yè)中��,這類生物制品通常是通過在特定宿主細胞中表達目標(biāo)基因來生產(chǎn)的�����。這些宿主細胞的類型多樣��,包括細菌(例如大腸桿菌)���、酵母、昆蟲細胞和哺乳動物細胞等����。 然而在實際生產(chǎn)和純化過程中�����,宿主細胞DNA往往會不可避免地遷移到最終產(chǎn)品中�,由于其可能導(dǎo)致安全性問題(如潛在的基因毒性或免疫反應(yīng))��,因此����,監(jiān)管機構(gòu)通常會制定嚴格的宿主細胞DNA殘留限制標(biāo)準(zhǔn),以確保生物制品的安全性和有效性�。

宿主DNA殘留標(biāo)準(zhǔn)
我國藥典及美國FDA均對宿主殘留DNA量進行明文規(guī)范:例如2020版《中國藥典》明確規(guī)定用Vero細胞生產(chǎn)人用狂犬病疫苗,Vero細胞DNA殘留應(yīng)不高于3ng/劑�;基于Vero細胞的脊髓灰質(zhì)炎疫苗,DNA殘留量不高于50pg/劑�;基于CHO細胞的乙肝疫苗,DNA殘留量不高于10pg/劑����。
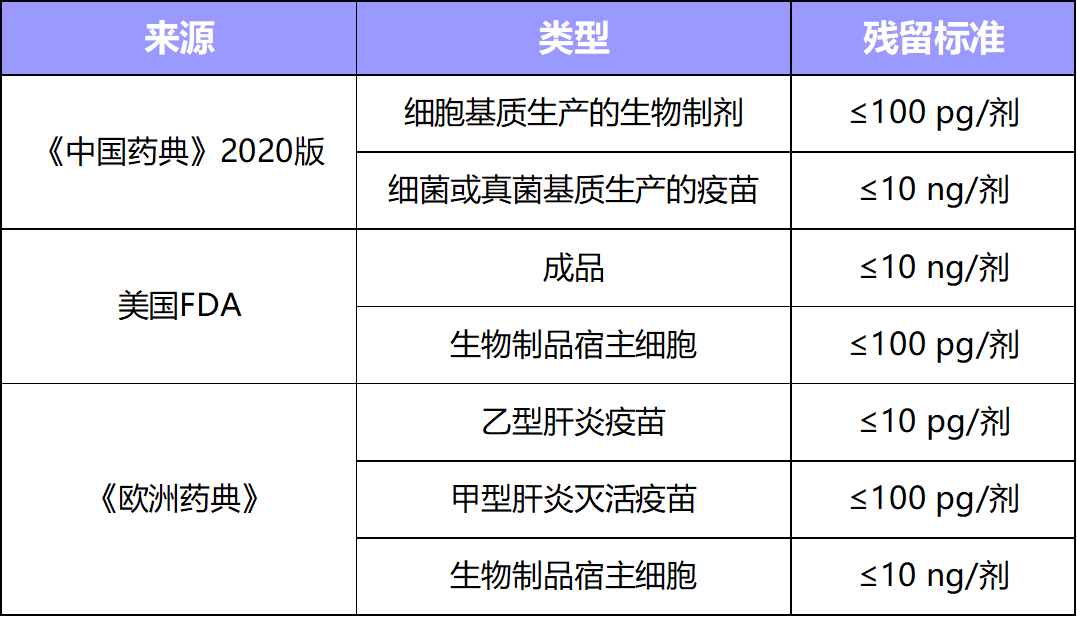
表 宿主細胞殘留DNA的限定標(biāo)準(zhǔn)
隨著技術(shù)的發(fā)展,人們認識到����,除了要減少殘留DNA的量�,也應(yīng)該降低宿主DNA片段的大小至功能基因大?����。ù蠹s200bp)以下��,從而減少致瘤性和感染性風(fēng)險�。 基于此,CDE 2022年5月發(fā)布的《體內(nèi)基因治療產(chǎn)品藥學(xué)研究與評價技術(shù) 指導(dǎo)原則(試行)》中明確指出���,生產(chǎn)若使用了腫瘤細胞系(如Hela細胞)����、致瘤細胞系���,或攜帶有致瘤基因����、病毒來源序列的細胞(如HEK 293T細胞)���,在確保無完整活細胞殘留的同時,需對DNA的殘留量和殘留片段大小進行控制,合理擬定標(biāo)準(zhǔn)限度�����。如有可能��,建議盡量將殘留DNA控制在10ng/劑以內(nèi)��, DNA殘留片段的大小控制在200bp以下���。
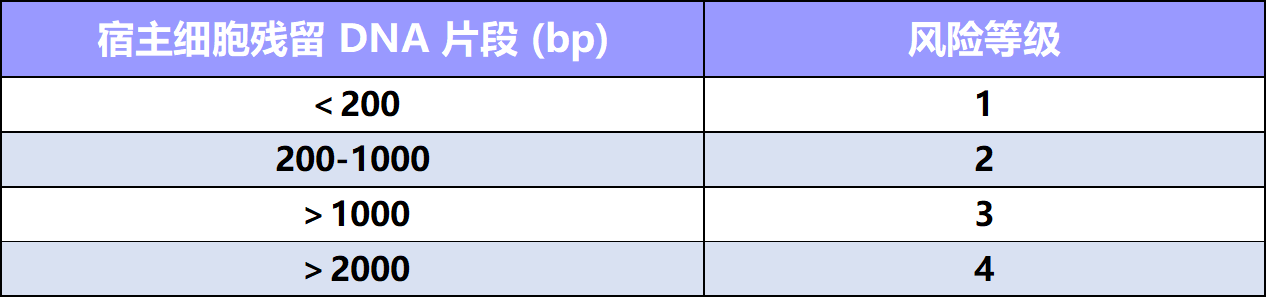
表 宿主細胞殘留DNA片段風(fēng)險等級
去除宿主DNA常見方法
宿主DNA的去除可以通過多種方法實現(xiàn)�,每種方法都有其特定的優(yōu)缺點�,目前常見的方法主要為層析法、酶法��、沉淀法等��。傳統(tǒng)單一的方法均存在核酸殘留去除不凈�����、工作量大����、耗時長等缺陷�,廣譜核酸酶則可完美解決此類難點���。
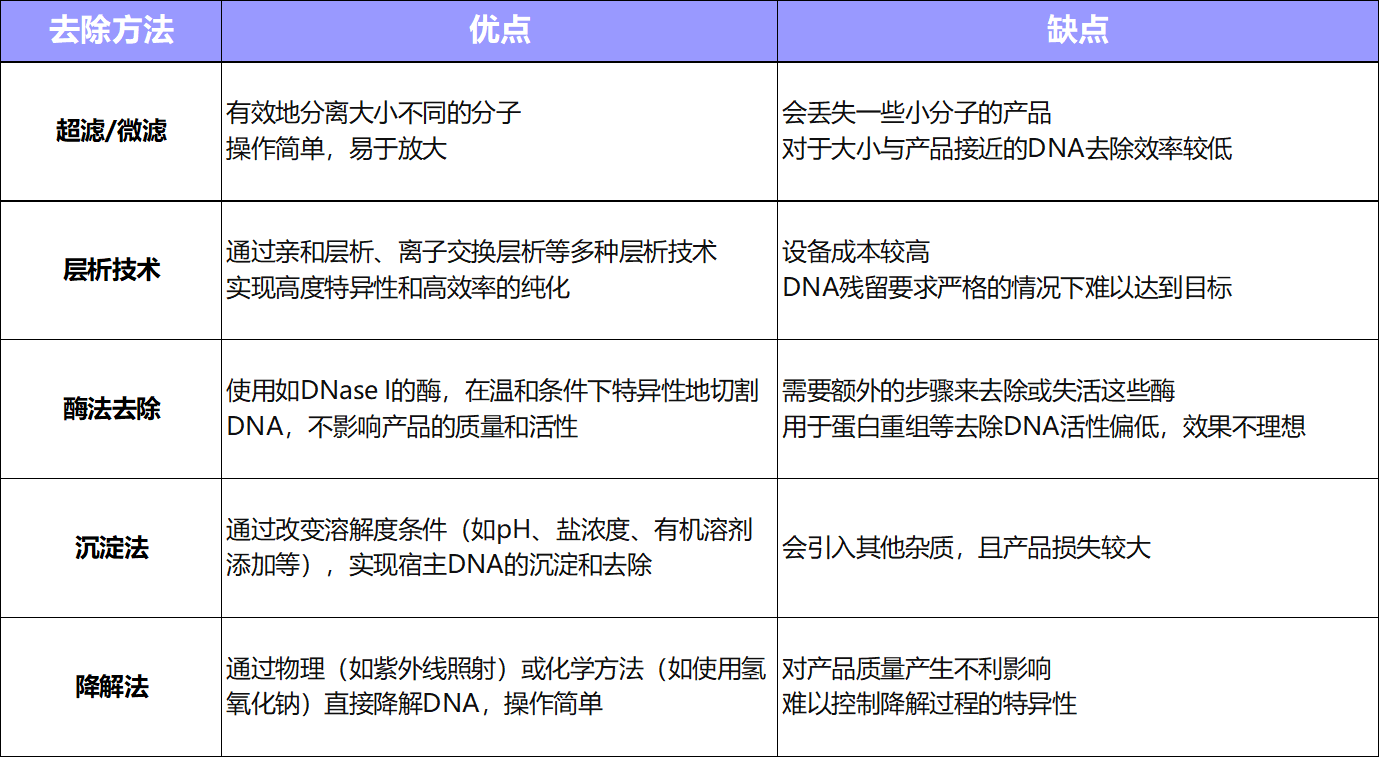
廣譜核酸酶�����,又稱為全能核酸酶����,一種來源于粘質(zhì)沙氏菌(Serratia marcescens�,又稱靈桿菌)的非特異性核酸內(nèi)切酶,它不含有原核生物表達的細菌內(nèi)毒素��。無論是實驗研究還是工業(yè)生產(chǎn)����,廣譜核酸酶都是目前少有能夠同時高效降解任何形式DNA和RNA的酶。
廣譜核酸酶的使用與優(yōu)勢
廣譜核酸酶能夠降解所有形式的DNA和RNA�,包括單鏈、雙鏈��、線性���、超螺旋和環(huán)狀DNA�����、RNA及基因組DNA��,對核酸序列沒有特異性���。在純化工藝中使用廣譜核酸酶,可有效降低細胞裂解液粘度���,改善蛋白純化工藝����,高效去除重組蛋白制品核酸污染�,大幅降低終產(chǎn)品污染風(fēng)險,滿足法規(guī)要求���,在細胞治療���、病毒載體疫苗等領(lǐng)域應(yīng)用廣泛。
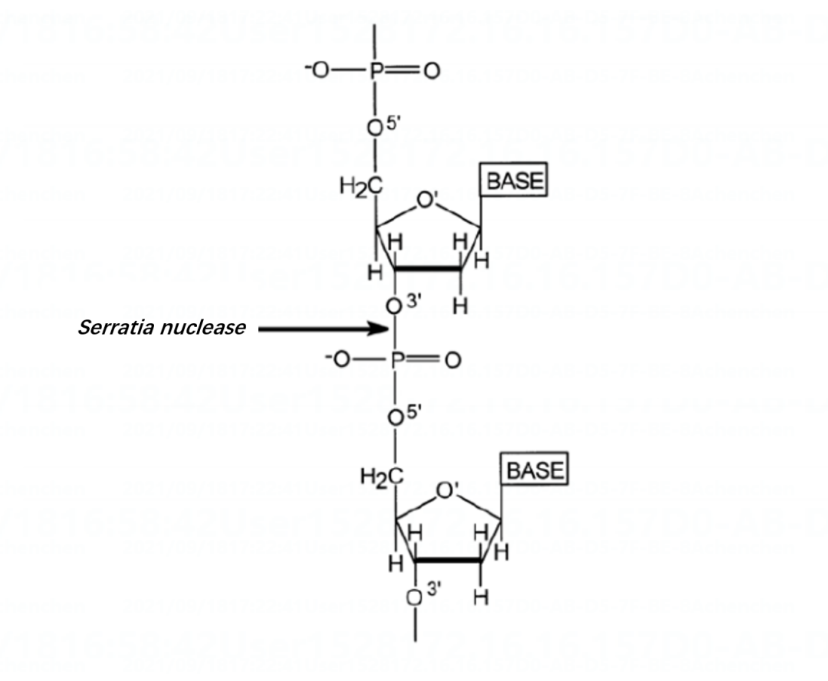
核酸酶的作用位點
廣譜核酸酶在廣泛的條件下仍有很強的生物酶活性�,跟大多數(shù)生物酶一樣,核酸酶的活性也會隨溫度���、pH值���、Mg2+�、緩沖體系和底物濃度等因素的改變而變化��。對于廣譜核酸酶使用方法���,可以點擊小編之前發(fā)布的文章《干貨分享| 廣譜核酸酶的使用�����,你學(xué)會了嗎��?》進行了解���。
相關(guān)產(chǎn)品
高度穩(wěn)定性
比活性大于1000 KU/mg蛋白
無動物源性成分
避免原核細胞的內(nèi)毒素污染
不含蛋白酶殘留
供應(yīng)穩(wěn)定,到貨快