抗體應(yīng)用和技術(shù)

抗體是用于各種實驗室技術(shù)的強大研究工具。在此���,我們將簡要介紹最流行的實驗室技術(shù)����,重點介紹它們?nèi)绾问褂每贵w。
酶聯(lián)免疫吸附實驗(ELISA)
ELISA是一種基于平板的技術(shù)��,可以檢測生物樣本中的抗原���。與其他免疫測定方法一樣��,ELISA依靠抗體與抗原的高度特異性相互作用來檢測目標(biāo)抗原��。ELISA可以對分析物和分子相互作用進(jìn)行定量和定性��。
在酶聯(lián)免疫吸附實驗中�,抗原被直接固定在固體表面上�����,或者更常見的是通過捕獲抗體固定在表面上(圖1)��。表面經(jīng)過洗滌�,然后與酶或熒光團(tuán)等分子連接的檢測抗體一起孵育�����。
在抗原存在的情況下,這些檢測抗體會與平板保持結(jié)合����,產(chǎn)生信號。信號的強度與樣本中的抗原濃度相對應(yīng)���。

圖1:夾心酶聯(lián)免疫吸附實驗裝置�����。多孔板上的捕獲抗體將固定感興趣的抗原��。與生物素和鏈霉親和素-HRP結(jié)合的檢測抗體將識別并結(jié)合該抗原��。
ELISA通常在多孔板(96孔或384孔)中進(jìn)行�,分析物的固定化有助于將抗原與其他樣品成分分離�����。這些特點使ELISA成為最容易同時對多個樣品進(jìn)行檢測的方法之一��。
酶聯(lián)免疫吸附法主要有四種:直接法��、間接法、夾心法和競爭法�,每種方法都有其獨特的優(yōu)缺點和適用性。每種實驗最合適的酶聯(lián)免疫吸附實驗形式取決與許多因素�����,包括所需的靈敏度��、特異性和檢測時間�����。
酶聯(lián)免疫斑點檢測
酶聯(lián)免疫斑點(ELISPOT)用于檢測細(xì)胞分泌的蛋白質(zhì)��,如細(xì)胞因子和生長因子�����。該技術(shù)可以量化和比較對各種刺激的免疫反應(yīng)�。
將細(xì)胞培養(yǎng)在96孔板中,使用抗體包被的PVDF或硝酸纖維素膜��。使用一抗和共軛二抗檢測相關(guān)分泌蛋白�����。分泌相關(guān)蛋白的細(xì)胞會出現(xiàn)色斑或熒光�����。掃描并分析膜��,量化分泌蛋白質(zhì)的細(xì)胞數(shù)量或比例�����。
免疫印跡(WB)
免疫印跡技術(shù)廣泛應(yīng)用于分離和鑒定蛋白質(zhì)的研究��。通過免疫印跡�,我們可以檢測蛋白質(zhì),確定不同樣本之間的相對蛋白質(zhì)水平����,并確定目標(biāo)蛋白質(zhì)的分子量,從而深入了解蛋白質(zhì)的翻譯后加工過程�。
免疫印跡包括三個主要步驟:(1)按大小分離蛋白質(zhì),(2)將蛋白質(zhì)轉(zhuǎn)移到膜上���,(3)使用一抗和二抗觀察目標(biāo)蛋白質(zhì)(圖2)�����。
第一步��,將蛋白質(zhì)裝載到凝膠上�,通過凝膠電泳按大小進(jìn)行分離。然后利用電流將蛋白質(zhì)條帶遷移到膜上����。蛋白質(zhì)轉(zhuǎn)移到膜上至關(guān)重要,因為用于電泳的凝膠為隨后的免疫染色提供了一個較差的表面�,即抗體不會粘附在凝膠的蛋白質(zhì)上。
最后�,用特異性抗體對膜進(jìn)行進(jìn)一步免疫染色,并用二抗和檢測試劑對膜進(jìn)行顯像�����。
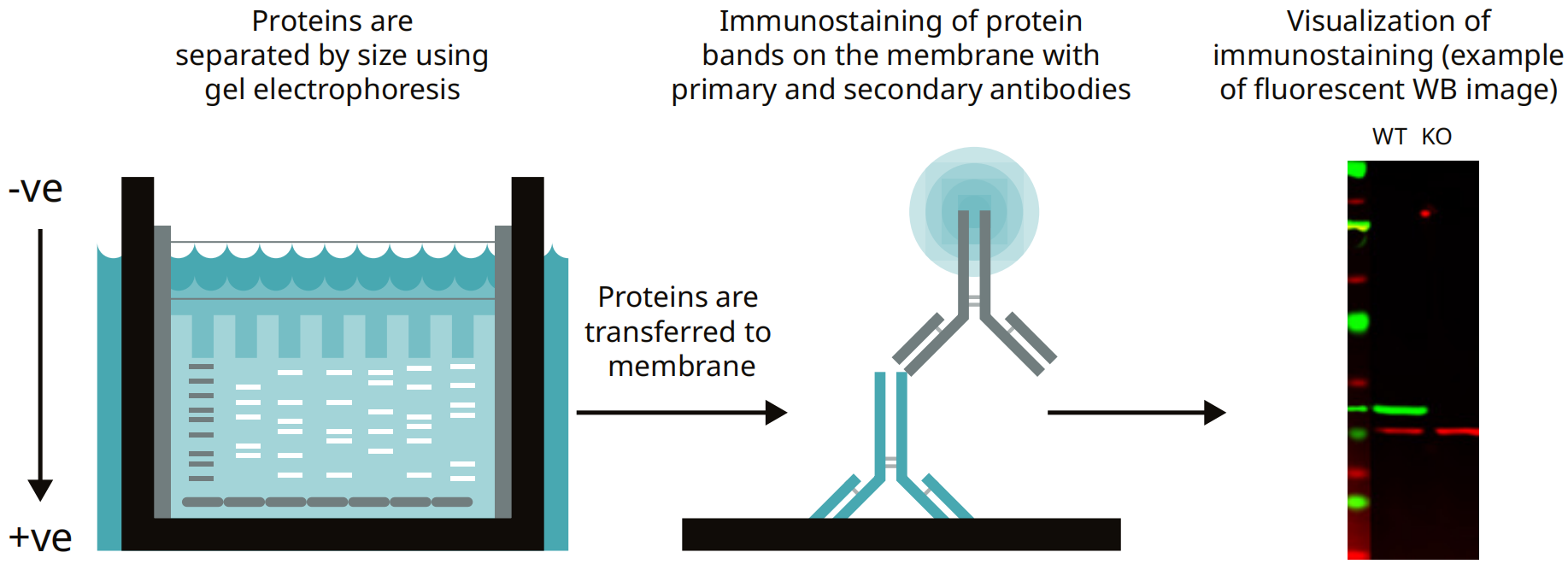
圖2:免疫印跡簡圖
免疫沉淀(IP)和染色質(zhì)免疫沉淀(ChIP)
免疫沉淀(IP)是一種分離和純化單個蛋白質(zhì)和復(fù)合蛋白質(zhì)的多功能技術(shù)��。在這項技術(shù)中�����,抗體被固定在固相基質(zhì)(如磁珠/瓊脂糖珠)上�,從復(fù)雜的溶液中捕捉抗原。
染色質(zhì)免疫沉淀(ChIP)用于確定特定蛋白質(zhì)是否與體內(nèi)特定DNA序列結(jié)合����。通過ChIP�����,研究人員可以確定感興趣的蛋白質(zhì)在整個基因組中結(jié)合的特定基因和系列,為了解其調(diào)控功能和機制提供重要線索�����。

圖3:ChIP方案工作流程���。進(jìn)行ChIP實驗的步驟:1.交聯(lián)�����,2.染色質(zhì)片段化��,3.免疫沉淀����,4.DNA 回收和純化��,5.DNA 分析��。
免疫組織化學(xué)(IHC)
免疫組織化學(xué)(IHC)是一種利用抗體-抗原相互作用來檢測組織切片中抗原分布和定位的方法(圖4)。雖然定量效果不如免疫印跡或ELISA���,但I(xiàn)HC具有在完成組織中鑒定蛋白質(zhì)表達(dá)的優(yōu)勢�����。
IHC通常用于診斷癌癥等疾病的組織異常�,IHC提供了寶貴的視角和支持���。
IHC染色依賴于能識別目標(biāo)抗原的抗體��。您可以使用顯色或熒光檢測系統(tǒng)來觀察抗體于抗原之間的相互作用���。在色原檢測中,抗體與酶結(jié)合����,當(dāng)抗體接觸色原是會產(chǎn)生彩色沉淀。在熒光檢測中��,抗體與熒光團(tuán)結(jié)合����。樣品制備和可視化技術(shù)多種多樣��,所使用的方法應(yīng)根據(jù)樣本類型和所需的靈敏度而定����。

圖4:左圖為正常人扁桃體組織(福爾馬林固定石蠟包埋切片)的熒光多重IHC染色�����?����?筆D1(橙色)�、抗PDL1(綠色)�、抗CD68(黃色)、抗CD3(紅色)��、抗Ki67(淡藍(lán)色)和抗PanCK(灰色)的合并染色�����。右圖為用抗Ki67抗體對福爾馬林固定石蠟包埋的正常人扁桃體切片進(jìn)行IHC染色�����。
免疫細(xì)胞化學(xué)(ICC)
免疫細(xì)胞化學(xué)(ICC)是利用標(biāo)記抗體研究蛋白質(zhì)的亞細(xì)胞分布。與IHC不同的是���,這種技術(shù)側(cè)重于細(xì)胞樣本而不是組織塊�。
在ICC染色中��,針對相關(guān)蛋白質(zhì)的抗體被應(yīng)用于經(jīng)過固定和通透處理的細(xì)胞培養(yǎng)樣本���。ICC有兩種類型:直接和間接��。直接ICC使用的是共軛的一抗����,而間接ICC使用的是未共軛的一抗���,然后用共軛的二抗進(jìn)行檢測(圖5)�����。在大多數(shù)ICC實驗中��,抗體都用熒光團(tuán)標(biāo)記���,非常適合共定位研究�。各種成像技術(shù)���,如寬場顯微鏡����、共聚焦顯微鏡或旋轉(zhuǎn)圓盤顯微鏡都可用于檢測信號��。

圖5:左圖是用抗PDGFRA抗體(用Alexa Flour®488二抗檢測-綠色)和抗微管蛋白抗體(用Alexa Fluor®594二抗檢測-紅色)對SH-SY5Y細(xì)胞進(jìn)行間接ICC染色�。右圖是用共軛的抗KRT14抗體(Alexa Fluor®647-紅色)和共軛的抗微管蛋白抗體(Alexa Fluor®488-綠色)進(jìn)行直接ICC檢測。細(xì)胞核用DAPI(藍(lán)色)染色����。上圖顯示野生型細(xì)胞中的相關(guān)信號���,下圖顯示基因敲除沒有的特定信號�����。圖像由共聚焦顯微鏡拍攝�。
流式細(xì)胞儀和熒光激活細(xì)胞分揀
流式細(xì)胞儀是一種常用的激光技術(shù)�,用于分析細(xì)胞或顆粒的特征(圖13)。該技術(shù)測量混合群體中與單個細(xì)胞結(jié)合的標(biāo)記抗體發(fā)出的熒光。此外����,不同細(xì)胞對光的散射也可用于確定它們的大小和特性。

圖6:流式細(xì)胞儀概覽�。
通過流式細(xì)胞儀,可以分析細(xì)胞表面和細(xì)胞內(nèi)分子的表達(dá)����,確定異質(zhì)細(xì)胞群中不同細(xì)胞類型的特征,評估分離亞群的純度�����,分析細(xì)胞大小和體積�。它可同時對單個細(xì)胞進(jìn)行多參數(shù)分析。
熒光激活細(xì)胞分揀(FACS)是流式細(xì)胞術(shù)的一種衍生技術(shù)����,它根據(jù)熒光標(biāo)記將細(xì)胞群物理分離成亞群。
參考文獻(xiàn)
1 Bonifacino, J.S., and Dell'Angelica, E.C. (2001). Immunoprecipitation. Curr. Protoc. Cell Biol. Chapter 7, Unit 7.2.
2 Harlow, E., and Lane, D. (1988). Antibodies: A Laboratory Manual. Cold Spring Harbor Laboratory Press.
3 Gundry, R.L., and White, M.Y. (2010). Immunoprecipitation. In: Protein Chromatography: Methods and Protocols, eds. R. Gundry and M.Y. White, pp. 189-203. Humana Press.
4 Towbin H, Staehelin T, Gordon J. (1979) Electrophoretic transfer of proteins from polyacrylamide gels to nitrocellulose sheets: procedure and some applications. Proc Natl Acad Sci U S A. 76(9):4350-4.
5 Taylor, C. R., & Levenson, R. M. (2006). Quantification of immunohistochemistry—issues concerning methods, utility and semiquantitative assessment II. Histopathology, 49(4), 411-424.
6 Van Weemen, B. K., & Schuurs, A. H. (1971). Immunoassay using antigen-enzyme conjugates. FEBS letters, 15(3), 232-236.