
ACROBiosystems百普賽斯針對細(xì)胞治療生物制品的生產(chǎn)應(yīng)用需求����,設(shè)計(jì)開發(fā)了一系列性能經(jīng)過驗(yàn)證的高活性高質(zhì)量的重組蛋白產(chǎn)品�����。我們嚴(yán)格遵照國內(nèi)外細(xì)胞治療原輔料的各項(xiàng)法規(guī)要求��,依托GMP級別的生產(chǎn)廠房��,通過先進(jìn)的蛋白表達(dá)技術(shù),嚴(yán)格的工藝控制����,全面的質(zhì)量控制體系,保證批間一致性��,同時(shí)全方位全過程嚴(yán)格控制病毒����、支原體、細(xì)菌��、內(nèi)毒素等外源因子污染����,滿足法規(guī)要求。不僅可為已使用我司臨床前RUO或Premium級別試劑的藥物研發(fā)客戶提供臨床前Non-GMP級別關(guān)鍵試劑快速轉(zhuǎn)化為GMP級別產(chǎn)品的升級服務(wù)�,同時(shí),也可提供從臨床前研發(fā)階段Non-GMP級別蛋白開發(fā)到臨床GMP級別蛋白生產(chǎn)的一站式開發(fā)服務(wù)��,更好滿足細(xì)胞治療藥物各開發(fā)階段及應(yīng)用場景需求�����,全面加速您的藥物研發(fā)進(jìn)程���。
ACRO GMP級別蛋白產(chǎn)品定制服務(wù)的優(yōu)勢

先進(jìn)的重組蛋白開發(fā)平臺
①針對細(xì)胞治療應(yīng)用進(jìn)行蛋白結(jié)構(gòu)設(shè)計(jì)���,保證優(yōu)秀的產(chǎn)品性能��。
②豐富的蛋白表達(dá)技術(shù)平臺和放大生產(chǎn)經(jīng)驗(yàn)�。
③5,000+性能經(jīng)過驗(yàn)證的標(biāo)準(zhǔn)重組蛋白產(chǎn)品在線��,支持從RUO快速升級轉(zhuǎn)換成GMP級別產(chǎn)品��。
④全面的蛋白活性分析和應(yīng)用場景性能確認(rèn)檢測平臺�。

GMP級別生產(chǎn)平臺
①成熟的GMP質(zhì)量管理體系。
②無動(dòng)物源性生產(chǎn)過程�,全方位全過程嚴(yán)格控制病毒���、支原體�����、細(xì)菌���、內(nèi)毒素等外源因子污染。
③先進(jìn)的工藝控制水平及全面的質(zhì)量控制和嚴(yán)格的產(chǎn)品放行流程確保蛋白產(chǎn)品批間一致性�。
加速臨床/上市申報(bào)
①專為細(xì)胞治療臨床應(yīng)用設(shè)計(jì)。
②嚴(yán)格遵照國內(nèi)外細(xì)胞治療原輔料的各項(xiàng)法規(guī)。
③支持線上/線下審計(jì)�。
④完善的生產(chǎn)批記錄等相關(guān)文檔。
GMP級別蛋白的一站式開發(fā)服務(wù)
技術(shù)先進(jìn)且質(zhì)控全面的蛋白設(shè)計(jì)和開發(fā)平臺
ACROBiosystems百普賽斯針對細(xì)胞治療應(yīng)用進(jìn)行針對性的蛋白結(jié)構(gòu)設(shè)計(jì)�,提供從基因合成、載體構(gòu)建到蛋白質(zhì)表達(dá)�����、純化的一站式服務(wù)��,可以根據(jù)客戶需求�����,選用不同表達(dá)/純化標(biāo)簽�、表達(dá)宿主等,滿足您的不同研究需求��,并最大限度提高研究項(xiàng)目的成功率��。對于Non-GMP級別產(chǎn)品�,我們?nèi)允褂枚喾N應(yīng)用場景和分析技術(shù)進(jìn)行產(chǎn)品性能驗(yàn)證,確保制備的的關(guān)鍵物料滿足您后續(xù)研發(fā)要求��。同時(shí)�����,我們的生產(chǎn)工藝可放大,GMP級別蛋白產(chǎn)品可使用與Non-GMP級別蛋白相同的克隆�����、序列和表達(dá)系統(tǒng)���,具有相同的性能�����,使您的關(guān)鍵物料實(shí)現(xiàn)向GMP級別的無縫轉(zhuǎn)換���。我們可以將現(xiàn)有的目錄Non-GMP級別蛋白產(chǎn)品轉(zhuǎn)化為GMP級別,也可以從零開始為您提供從頭定制化開發(fā)服務(wù)�����。
專業(yè)的蛋白表達(dá)技術(shù)平臺(真核/原核)
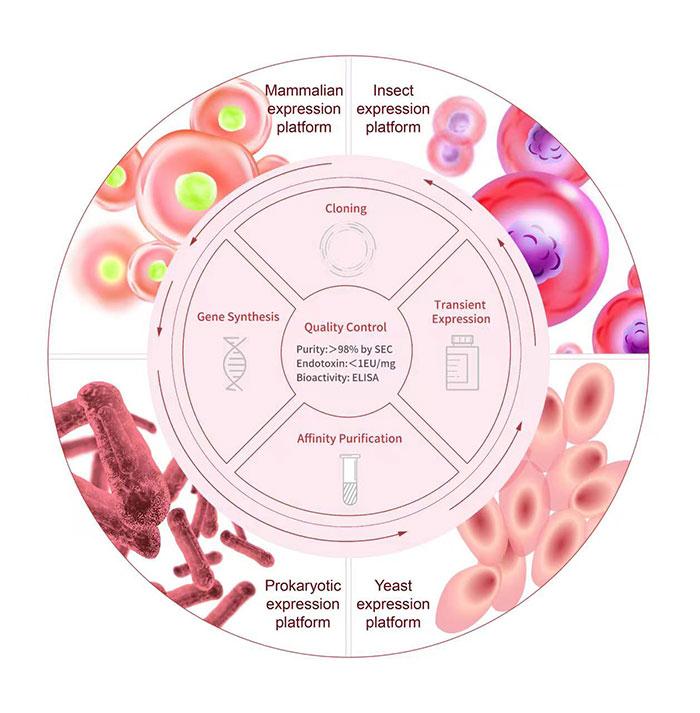
行業(yè)領(lǐng)先的GMP重組蛋白開發(fā)平臺
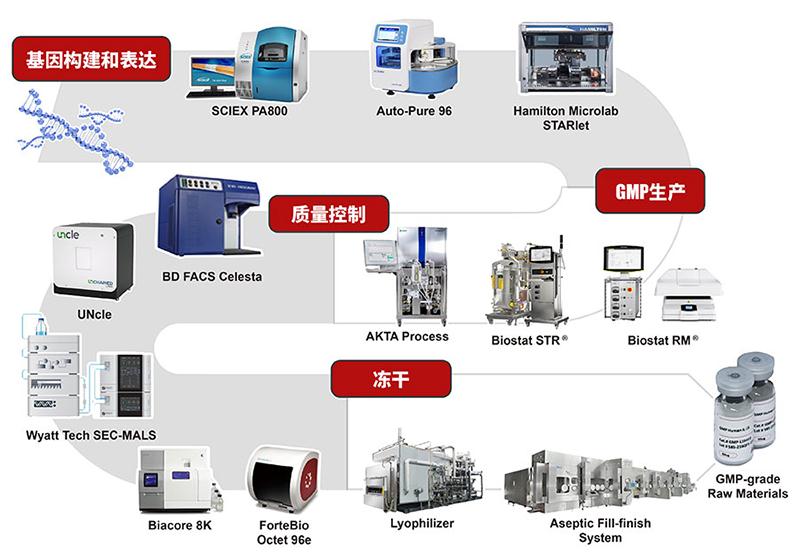
臨床前關(guān)鍵物料的GMP轉(zhuǎn)化升級服務(wù)
ACROBiosystems百普賽斯具有超10年的重組蛋白開發(fā)經(jīng)驗(yàn)���,我們依托多種重組蛋白表達(dá)系統(tǒng),包括昆蟲細(xì)胞�����、哺乳動(dòng)物細(xì)胞和原核蛋白表達(dá)系統(tǒng),目前已擁有5,000多種重組蛋白產(chǎn)品�����,其中包括Non-GMP及GMP不同級別的產(chǎn)品���。為了更好地實(shí)現(xiàn)從臨床前開發(fā)到臨床階段的無縫過渡����,我們建議您在臨床前研究期間盡早確定合適的關(guān)鍵原料����,您可以在早期研發(fā)階段使用ACROBiosystems百普賽斯開發(fā)的Non-GMP級別原料,它與GMP 級別具有同樣的性能�����,后續(xù)進(jìn)入CMC或者臨床時(shí)����,您只需選擇成我們的GMP級別生產(chǎn)服務(wù),即可快速輕松過渡到臨床階段�����。
成熟的GMP質(zhì)量管理體系
藥品生產(chǎn)質(zhì)量管理規(guī)范(Good Manufacturing Practice,GMP)是藥監(jiān)局為生產(chǎn)優(yōu)良藥品而制定的關(guān)于人員�����、廠房設(shè)施與設(shè)備���、生產(chǎn)管理質(zhì)量管理以及文件管理等方面的標(biāo)準(zhǔn)規(guī)則����。它是一套適用于制藥等行業(yè)的強(qiáng)制性標(biāo)準(zhǔn)�����,是藥品生產(chǎn)和質(zhì)量管理的基本準(zhǔn)則�����。適用于藥品生產(chǎn)的全過程和原料藥生產(chǎn)中影響成品質(zhì)量的關(guān)鍵工序�����。它是一種先進(jìn)的管理系統(tǒng)���,廣泛應(yīng)用于藥品安全生產(chǎn)過程中���,要求藥品生產(chǎn)企業(yè)擁有良好的生產(chǎn)設(shè)備、合理的生產(chǎn)工藝��、完善的質(zhì)量管理和嚴(yán)格的檢測制度��,確保產(chǎn)品質(zhì)量符合相關(guān)標(biāo)準(zhǔn)��,并能及時(shí)發(fā)現(xiàn)生產(chǎn)過程中存在的問題�����,加以改善�。
為了更好的支持細(xì)胞治療相關(guān)客戶,ACROBiosystems百普賽斯于2021年針對GMP級別產(chǎn)品建立了嚴(yán)格的GMP質(zhì)量管理體系�����。通過體系有效運(yùn)行�����,可以確保產(chǎn)品和服務(wù)的質(zhì)量得到有效的保證���。
全自動(dòng)灌裝設(shè)備

滅菌設(shè)備

全方位質(zhì)量放行平臺加速臨床/上市申報(bào)
由于蛋白質(zhì)是在生物系統(tǒng)中生產(chǎn)的��,制造環(huán)境或工藝的變化會使其容易出現(xiàn)批次間的差異���。為了確保一致性�����,除了在生產(chǎn)制造環(huán)節(jié)給予特別關(guān)注�����,對于生物制品穩(wěn)定性及批間一致性更需要多種質(zhì)量控制手段進(jìn)行放行���,才能最大程度確保關(guān)鍵物料的安全及有效性。
ACROBiosystems百普賽斯具有強(qiáng)大的蛋白質(zhì)分析平臺�,可以對產(chǎn)品進(jìn)行全面的質(zhì)量性能測試,確保質(zhì)量穩(wěn)定可靠���,并全程嚴(yán)格控制外源因子污染���,嚴(yán)格保證安全性(無菌,支原體,外源病毒��,內(nèi)毒素等)符合法規(guī)要求��。
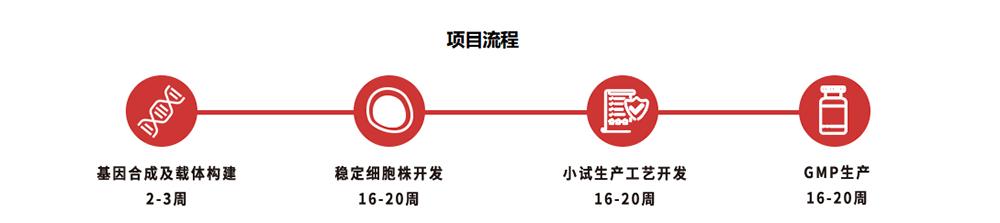
關(guān)鍵字: GMP蛋白定制;GMP細(xì)胞因子定制;重組蛋白定制服務(wù);蛋白定制服務(wù);GMP級別細(xì)胞因子;
百普賽斯集團(tuán)ACROBiosystems Group(股票代碼:301080)是成立于2010年的跨國生物科技公司����,是為全球生物醫(yī)藥�、健康產(chǎn)業(yè)領(lǐng)域提供關(guān)鍵生物試劑產(chǎn)品及解決方案的行業(yè)平臺型基石企業(yè)。2021年在創(chuàng)業(yè)板上市���。百普賽斯集團(tuán)業(yè)務(wù)遍布全球��,橫跨亞洲�、北美洲����、歐洲,在中國�、美國、瑞士等12個(gè)城市設(shè)有辦公室��、研發(fā)中心及生產(chǎn)基地�����。目前累計(jì)服務(wù)客戶超6000家,與全球Top 20醫(yī)藥企業(yè)均建立了長期�、穩(wěn)定的合作伙伴關(guān)系。集團(tuán)旗下?lián)碛衅放艫CROBiosystems百普賽斯�、bioSeedin柏思薈、Condense Capital墾拓資本和ACRODiagnostics百斯醫(yī)學(xué)等����。